Découverte de l’acide hyaluronique.
De l’oeil à l’articulation.
Du décollement de rétine à l’arthrose.
En préambule,
L’acide hyaluronique (AH) est aujourd’hui d’utilisation courante en médecine. Ses premières applications chez l’homme ont été réalisées en ophtalmologie et ce sont d’ailleurs les spécialistes de cette discipline médicale associés à des biochimistes et des physiciens qui ont mis au point les premières solutions après en avoir précisé la nature et la fonction. A partir des années 1970, l’utilisation de cette substance à caractère ubiquitaire dans le monde animal est devenue de plus en plus courante à mesure que l’industrie offrait des produits adaptés aux besoins notamment de la rhumatologie, de l’ophtalmologie, de l’urologie ou de la dermatologie. Aujourd’hui la viscosupplémentation dans l’arthrose est bien codifiée et tout s’oriente vers la préparation de nouveaux gels plus stables et donc moins dégradables pour limiter le nombre des injections dans le temps et augmenter l’action antalgique et fonctionnelle avec l’espoir que ce traitement montrera dans les quelques années qui viennent son effet protecteur sur les tissus dans lequel il est injecté du fait de ses propriétés pharmacologiques de plus en plus connues et étonnantes. Qualifié de traitement symptomatique de l’arthrose l’AH va-t-il devenir la chaine de protection du cartilage ?
Nous allons évoquer en quelques lignes…
…l’histoire de sa découverte de à travers plus d’un siècle de recherches réparties entre de nombreux pays. Plus qu’une approche physico-chimique de cette substance, nous évoquerons les différentes étapes qui ont amené à la naissance des gels qui nous sont proposés aujourd’hui.
Cela remonte au siècle dernier et la première approche de la substance peut être attribuée au chimiste français Portes qui, en 1880, fait la remarque que le corps vitreux de l’œil n’a pas la même consistance que la cornée ou le cartilage. ll donne le nom de hyalomucine au constituant de cette loge de l’oeil.
Dans cette fin de siècle on s’intéresse beaucoup aux carbohydrates dont la formule générale correspond à Cⁿ(H₂O)ⁿ et on les repère avec des colorations sur des coupes tissulaires et histologiques au microscope qui commence à être très en vogue. C’est en effet aussi l’explosion de la chimie des colorants et des tissus dont la soie naturelle. En 1889 Mörner met donc en évidence la présence de carbohydrate dans une substance mucoïde extraite du cartilage qui sera plus tard définie comme un polysaccharide : le sulfate de chondroïtine. En 1916 McLean isole un anticoagulant, l’héparine, que Howell va classer dans les carbohydrates. Puis Levene en 1918 isole un autre polysaccharide dans lequel il trouve une glucosamine et un acide glucuronique sulfaté qu’il appelle acide mucoïtine sulfurique. C’est probablement l’acide hyaluronique que l’on vient de découvrir mais avec une erreur de jeunesse «sulfatée». En 1929 l’espagnol F. Duran-Reynals met en évidence dans des extraits de testicule la présence de facteurs de diffusion (la future hyaluronidase) qui détruisent le tissu conjonctif sous cutané permettant dans son expérience la diffusion de l’encre de Chine. Tous les ingrédients sont alors réunis pour permettre la découverte de l’AH.
Ainsi en 1934, à l’université de Columbia de New York…
…dans le département d’ophtalmologie, Karl Meyer et John Palmer décrivent ce nouveau polysaccharide isolé de l’humeur vitrée d’un œil de bœuf et contenant un acide uronique «non sulfaté» lié à un hexosamine. Ils l’appellent acide hyaluronique parce qu’isolé comme un acide, et « hyal » pour vitreux en grec. En fait il se trouve à l’état de sel de sodium dans les conditions physiologiques. Ils découvrent plus tard la même substance, comme d’autres équipes, dans le liquide synovial, le cartilage, la peau, le cordon ombilical, la crête de coq. De son coté, F.E.Kendall, en 1937, met en évidence la même substance polysaccharidique sur la capsule de certaines bactéries du groupe des streptocoques hémolytiques A. Cette découverte va être plus tard à l’origine de la fabrication bactérienne de l’acide hyaluronique quand la technique d’extraction aura été améliorée en 1974 dans un premier temps par John Scott. Quelques années sont encore nécessaires à Karl Meyer alors associé à B Weissmann pour écrire en 1952 la structure chimique de l’acide hyaluronique grâce aux différentes hyaluronidases qu’il a classé et qui ont permis de fragmenter progressivement cette longue chaine hydrocarbonée. Albert Dorfman de Chicago avait de son coté isolé aussi ces enzymes en 1951 dont l’ enzyme testiculaire déjà évoquée avec les facteurs de diffusion de F. Duran-Reynals cité plus haut. C’est aussi lui qui présentera après John Scott en 1979 une technique plus sûre d’extraction de l’AH depuis les parois des streptocoques A. La structure de l’AH bénéficie aussi des nouvelles techniques d’exploration dont le microscope électronique et Fessler en 1966 montre une première « vision » de cette immense chaine hydrocarbonée pressentie dans les travaux antérieurs. John Scott en 1978 revient en scène pour décrire l’existence de ponts d’hydrogène liant les chaines entre elles permettant ainsi d’éviter leur oxydation, ce qui est confirmé par la RMN ensuite. L’acide hyaluronique est donc bien cette double chaine hydrocarbonée hélicoïdale qui a déjà été décrite par Atkins en 1962.
lié à un hexosamine. Ils l’appellent acide hyaluronique parce qu’isolé comme un acide, et « hyal » pour vitreux en grec. En fait il se trouve à l’état de sel de sodium dans les conditions physiologiques. Ils découvrent plus tard la même substance, comme d’autres équipes, dans le liquide synovial, le cartilage, la peau, le cordon ombilical, la crête de coq. De son coté, F.E.Kendall, en 1937, met en évidence la même substance polysaccharidique sur la capsule de certaines bactéries du groupe des streptocoques hémolytiques A. Cette découverte va être plus tard à l’origine de la fabrication bactérienne de l’acide hyaluronique quand la technique d’extraction aura été améliorée en 1974 dans un premier temps par John Scott. Quelques années sont encore nécessaires à Karl Meyer alors associé à B Weissmann pour écrire en 1952 la structure chimique de l’acide hyaluronique grâce aux différentes hyaluronidases qu’il a classé et qui ont permis de fragmenter progressivement cette longue chaine hydrocarbonée. Albert Dorfman de Chicago avait de son coté isolé aussi ces enzymes en 1951 dont l’ enzyme testiculaire déjà évoquée avec les facteurs de diffusion de F. Duran-Reynals cité plus haut. C’est aussi lui qui présentera après John Scott en 1979 une technique plus sûre d’extraction de l’AH depuis les parois des streptocoques A. La structure de l’AH bénéficie aussi des nouvelles techniques d’exploration dont le microscope électronique et Fessler en 1966 montre une première « vision » de cette immense chaine hydrocarbonée pressentie dans les travaux antérieurs. John Scott en 1978 revient en scène pour décrire l’existence de ponts d’hydrogène liant les chaines entre elles permettant ainsi d’éviter leur oxydation, ce qui est confirmé par la RMN ensuite. L’acide hyaluronique est donc bien cette double chaine hydrocarbonée hélicoïdale qui a déjà été décrite par Atkins en 1962.
 Des travaux intermédiaires ont d’autre part bien mis en évidence le métabolisme de l’acide hyaluronique dans l’organisme. Il ne persiste que quelques minutes dans la circulation générale, 24 heures dans la peau et quelques jours dans le cartilage. La fabrication articulaire est dédiée à des cellules de la membrane synoviale, les synoviocytes B ou hyalocytes qui tricotent l’acide hyaluronique. Il est synthétisé de façon tout à fait particulière à la face interne de la membrane cellulaire. Le polymère naissant est extrudé au travers de la membrane vers l’extérieur au fur et à mesure qu’il s’allonge par ajout alterné d’un acide glucuronique et d’une N-acétylglucosamine formant chaque maillon. La croissance sans limite du polymère est ainsi possible sans risque d’encombrement dans la cellule. Cette fabrication est permanente et modulée par des enzymes multigéniques ; les hyaluronane synthases (HAs) codées par des gènes différents en fonction des tissus. La dégradation est sous le contrôle d’une autre famille d’enzymes ; les hyaluronidases déjà citées plus haut : protéines dont la fabrication sous codage dépend de plusieurs autres gènes comme HIAL 1 et HIAL2 et dont la synthèse à été initiée par Frost en 1997. La fabrication bactérienne de l’AH est sous la dépendance du même processus ce qui explique la relative facilité avec laquelle on va pouvoir « récolter » le viscosupplément.
Des travaux intermédiaires ont d’autre part bien mis en évidence le métabolisme de l’acide hyaluronique dans l’organisme. Il ne persiste que quelques minutes dans la circulation générale, 24 heures dans la peau et quelques jours dans le cartilage. La fabrication articulaire est dédiée à des cellules de la membrane synoviale, les synoviocytes B ou hyalocytes qui tricotent l’acide hyaluronique. Il est synthétisé de façon tout à fait particulière à la face interne de la membrane cellulaire. Le polymère naissant est extrudé au travers de la membrane vers l’extérieur au fur et à mesure qu’il s’allonge par ajout alterné d’un acide glucuronique et d’une N-acétylglucosamine formant chaque maillon. La croissance sans limite du polymère est ainsi possible sans risque d’encombrement dans la cellule. Cette fabrication est permanente et modulée par des enzymes multigéniques ; les hyaluronane synthases (HAs) codées par des gènes différents en fonction des tissus. La dégradation est sous le contrôle d’une autre famille d’enzymes ; les hyaluronidases déjà citées plus haut : protéines dont la fabrication sous codage dépend de plusieurs autres gènes comme HIAL 1 et HIAL2 et dont la synthèse à été initiée par Frost en 1997. La fabrication bactérienne de l’AH est sous la dépendance du même processus ce qui explique la relative facilité avec laquelle on va pouvoir « récolter » le viscosupplément.
En Angleterre, à Oxford…
…,AG Ogston dans les années 1960-70 isole par ultra filtration l’AH du liquide synovial qui reste mêlé à près de 30% de protéines, en détermine la concentration à raison d’ 1 gramme par litre ainsi que le poids moléculaire autour de 4 Kdaltons. Il décrit la molécule comme une grande sphère hydratée composée de chaines arrangées en pelote qui lui donne cette viscosité si particulière. L’auteur explique le maillage entre les chaines par l’existence de nombreuses protéines de liaison. Il décrit en fait les ponts hydrogène trouvés quelques années plus tard par J. Scott.
Depuis 1938 en Hongrie…
…,Endre Balazs s’intéresse aux polysaccharides d’abord végétaux puis animaux. Il est invité à Stockholm en 1947 pour présenter ses travaux sur le développement cellulaire induit par l’acide hyaluronique. Il finit par immigrer dans ce pays et travaille à l’Institut Karolinska avec Hjalmar Holmgren. Il continue ses travaux notamment sur le rôle de l’AH dans le développement des tumeurs. En 1950 il est appelé par Edwin Dumphy, chef du département d’ophthalmologie de Harvard Medical School à Boston, pour organiser la recherche dans une nouvelle structure la «Retina Foundation». A partir de cette période Endre Balazs tout en poursuivant ses recherche dans l’œil humain et animal ( il découvre les hyalocytes dans l’humeur vitrée) va assurer la promotion, la publicité et le développement de l’AH dans diverses pathologies. D’ailleurs en 1962 à l’occasion du transfert de la fondation dans une autre structure, il obtient la possibilité d’étendre à d’autres domaines que l’œil ses recherches. En 1965 il crée l’Institut de recherche biomédicale de Boston dont il devient le président et va étendre ses compétences oculaires à la peau et aux articulations. L’AH devient une substance de routine en chirurgie ophtalmique. Balazs monte une petite structure de fabrication Biotrics Inc. qui produit le Healonnon. La société sera absorbée par le suédois Pharmacia en 1976 ( et ultérieurement Pfizer Inc) qui deviendra ainsi le leader mondial de l’AH avec Healon pour la chirurgie ophtalmique et l’arthrose. En 1980 avec sa femme et son fils, il recrée une société : Biomatrix Inc.. Elle va produire de nombreux acides hyaluroniques d’origine aviaire pour les besoins de la peau et des articulations. Balazs impose le terme de hyaluronan dans la nomenclature internationale pour l’acide hyaluronique à partir de 1986. Le Hylan G F 20 ou Synvisc mélange de 2 formulations d’AH est son fer de lance. Finalement la société est vendue à Genzyme Inc en 2000 aujourd’hui absorbée par Sanofi. Les travaux de Balazs restent aujourd’hui des références en matière de fabrication et de schéma thérapeutique. Actuellement aux USA , les HA sont présents avec Anika Therapeutics créé en 1993 avec Orthovisc. Cette société a absorbé il y a 2 ans l’italienne Fidia..
le rôle de l’AH dans le développement des tumeurs. En 1950 il est appelé par Edwin Dumphy, chef du département d’ophthalmologie de Harvard Medical School à Boston, pour organiser la recherche dans une nouvelle structure la «Retina Foundation». A partir de cette période Endre Balazs tout en poursuivant ses recherche dans l’œil humain et animal ( il découvre les hyalocytes dans l’humeur vitrée) va assurer la promotion, la publicité et le développement de l’AH dans diverses pathologies. D’ailleurs en 1962 à l’occasion du transfert de la fondation dans une autre structure, il obtient la possibilité d’étendre à d’autres domaines que l’œil ses recherches. En 1965 il crée l’Institut de recherche biomédicale de Boston dont il devient le président et va étendre ses compétences oculaires à la peau et aux articulations. L’AH devient une substance de routine en chirurgie ophtalmique. Balazs monte une petite structure de fabrication Biotrics Inc. qui produit le Healonnon. La société sera absorbée par le suédois Pharmacia en 1976 ( et ultérieurement Pfizer Inc) qui deviendra ainsi le leader mondial de l’AH avec Healon pour la chirurgie ophtalmique et l’arthrose. En 1980 avec sa femme et son fils, il recrée une société : Biomatrix Inc.. Elle va produire de nombreux acides hyaluroniques d’origine aviaire pour les besoins de la peau et des articulations. Balazs impose le terme de hyaluronan dans la nomenclature internationale pour l’acide hyaluronique à partir de 1986. Le Hylan G F 20 ou Synvisc mélange de 2 formulations d’AH est son fer de lance. Finalement la société est vendue à Genzyme Inc en 2000 aujourd’hui absorbée par Sanofi. Les travaux de Balazs restent aujourd’hui des références en matière de fabrication et de schéma thérapeutique. Actuellement aux USA , les HA sont présents avec Anika Therapeutics créé en 1993 avec Orthovisc. Cette société a absorbé il y a 2 ans l’italienne Fidia..
En France, JG. Peyron…
…, rhumatologue parisien et mondialement connu pour ses travaux dans l’arthrose et le cartilage voit très vite tout l’intérêt de l’acide hyaluronique et travaille avec Balazs. Ils publient une étude chez l’homme en 1974 après celle de Rydell sur les chevaux de course en 1966 et sur des sujets arthrosiques en 1972. Les résultats sont suffisamment encourageants pour être renouvelés à partir de cette époque. On voit ainsi apparaitre de nombreux travaux canadiens avec Adams et Lussier, suédois avec Lohmander, français avec Dougados. Ils s’étalent sur une vingtaine d’années tandis que se multiplient les sources d’acide hyaluronique au Japon, en France et en Suède. En 1990 le même Peyron introduit le concept de viscosupplémentation qui continue à prévaloir aujourd’hui. Chez nous l’acide hyaluronique a été introduit comme un médicament grâce à Hyalgan (un dérivé aviaire) produit par la firme italienne Fidia en 1995. Avant cette date les français passaient la frontière italienne, souvent à Vintimille, pour se fournir en viscosupplément et faire faire ensuite leurs injections. En 1997 c’est l’arrivée de Synvisc et la généralisation du traitement par viscosupplémentation pris en charge pour le genou par la sécurité sociale 6 ans plus tard en 2003. C’est en France que l’on ne tardera pas à partir des années 2000 à utiliser l’AH pour l’arthrose de hanche dans la foulée de la réintroduction des injections de corticoïdes. Elles étaient « devenues » dangereuses en cas de mise en place ultérieure d’une prothèse. En réalité, elles étaient efficaces, sans danger avec des conditions techniques parfaites et elles étaient souhaitées par de nombreux patients avant l’intervention ultime. Après un travail multicentrique en 2003 avec Hylan GF 20 sur la coxarthrose, la même équipe de E. Vignon avec T Conrozier et P. Mathieu a clairement proposé en 2005 la poursuite de la viscosupplémentation dans la hanche qui est alors devenu un geste courant parce qu’efficace dans ses indications précises.
En Suéde…
 …,pays de passage pour Balazs entre 1947 et 1950 c’est Toward Laurent et son équipe qui comme Ogston à Oxford, travaille sur l’acide hyaluronique à Upssala. Il précise, lui aussi, les relations entre cette substance et les proteines au sein des tissus conjonctifs, montre son rôle clé dans l’organisation des matrices péri et extracellulaires et la régulation des cellules qui y sont incluses. Mais il y a aussi Bengt Ågerup, physicien et chimiste qui travaille dès 1975 et durant une décennie chez Pharmacia au département d’ophtalmologie. Il développe le Healon d’origine aviaire en étroite collaboration avec Balazs pour la chirurgie de l’œil après le rachat de Biotrics. En 1985 il part de chez Pharmacia et devient consultant privé et crée la société Q.Med. Il est totalement convaincu de l’avenir des hyaluronans non animaux d’origine bactérienne et réticulés. Les produits du moment disparaissent en quelques jours et l’origine aviaire peut poser selon lui problème. Il travaille ainsi les week-ends dans la cuisine d’une maison à la campagne
…,pays de passage pour Balazs entre 1947 et 1950 c’est Toward Laurent et son équipe qui comme Ogston à Oxford, travaille sur l’acide hyaluronique à Upssala. Il précise, lui aussi, les relations entre cette substance et les proteines au sein des tissus conjonctifs, montre son rôle clé dans l’organisation des matrices péri et extracellulaires et la régulation des cellules qui y sont incluses. Mais il y a aussi Bengt Ågerup, physicien et chimiste qui travaille dès 1975 et durant une décennie chez Pharmacia au département d’ophtalmologie. Il développe le Healon d’origine aviaire en étroite collaboration avec Balazs pour la chirurgie de l’œil après le rachat de Biotrics. En 1985 il part de chez Pharmacia et devient consultant privé et crée la société Q.Med. Il est totalement convaincu de l’avenir des hyaluronans non animaux d’origine bactérienne et réticulés. Les produits du moment disparaissent en quelques jours et l’origine aviaire peut poser selon lui problème. Il travaille ainsi les week-ends dans la cuisine d’une maison à la campagne ( l’histoire est vraie et la maison est le siège de sa société : Q.Med ) pour mettre au point un produit que des urologues infantiles lui demandent afin de remplacer Teflon et silicone alors utilisés dans les reflux vésico-urinaires chez l’enfant. Après avoir obtenu en 1995 ce gel d’AH qui lui parait parfait, il dépose un brevet de « NASHA™ technology ». C’est ensuite la commercialisation de Restilane® pour la peau, Deflux™ pour l’urologie et Durolane® pour l’arthrose. La société Q Med vient d’être rachetée par Galderma un laboratoire de dermatologie partagé entre L’Oréal et Nestlé.
( l’histoire est vraie et la maison est le siège de sa société : Q.Med ) pour mettre au point un produit que des urologues infantiles lui demandent afin de remplacer Teflon et silicone alors utilisés dans les reflux vésico-urinaires chez l’enfant. Après avoir obtenu en 1995 ce gel d’AH qui lui parait parfait, il dépose un brevet de « NASHA™ technology ». C’est ensuite la commercialisation de Restilane® pour la peau, Deflux™ pour l’urologie et Durolane® pour l’arthrose. La société Q Med vient d’être rachetée par Galderma un laboratoire de dermatologie partagé entre L’Oréal et Nestlé.
Au Japon…
…, l’AH a été introduit très tôt en 1987 avec le Artz® ou Supartz® pour le traitement de l’arthrose du genou. C’est un dérivé de crête de coq mis au point par la firme japonaise Seikagaku Corporation et qui à ce jour a été le plus vendu dans le monde avec acceptation par la FDA en 2001. La firme a développé un Gel-One® monoinjection admis aux USA en 2011 et commercialisé par Zimmer.
Au Canada…
…, il y a eu de nombreux travaux avec notamment J.P. Pelletier et son épouse qui en 1993 suggère la viscosupplémentation comme traitement de l’arthrose ou M.E Adams et A.J Lussier en 1995 et 1996 qui ont décrit la séquence thérapeutique «idéale» pour la viscosupplémentation avec 1 injection par semaine pendant trois semaines de Hylan G.H. 20. Ce rythme s’est imposée ensuite aux autres préparations et fait, pour partie encore, référence. Aujourd’hui cette triple infiltration classique se discute avec l’apparition des mono injections qui trouvent une place dans certaines formes d’arthrose et de patients. D’autres comme Torrance en 2002 ont abordé dans leurs travaux le coût socio-économique (critère important dans la médecine au Canada) de la viscosupplémentation qui s’est avéré intéressant au regard des traitements classiques.
En conclusion,
Aujourd’hui la plupart des fournisseurs d’AH utilisent des préparations réalisées à partir de produits obtenus par fermentation bactérienne naturelle. Le composé obtenu est très pur généralement indemne de protéines étrangères à la différence des produits d’origine aviaire où ce risque immuno allergique potentiel connu et bien maitrisé n’en demeure pas moins plus élevé. Pendant que les travaux se poursuivent pour confirmer les capacités de l’AH à ralentir l’évolution de l’arthrose et à protéger le cartilage, la viscosupplémentation se développe avec l’apparition d’une seconde génération d’ AHs comportant une réticulation entre chaines partielle et contrôlée pour conserver ainsi toutes les propriétés mécaniques exceptionnelles de ce polysaccharide lorsqu’il se met en « boule » mais aussi antalgiques lorsqu’il est linéaire et disponible pour les récepteurs cellulaires. L’adjonction de sucres-alcool comme le mannitol que l’on trouve notamment dans HappyCross® ou le sorbitol qui augmentent la force des pontages entre chaines pour la fraction réticulée et diminue la dégradation oxydative pour celles restées libres, est un moyen nouveau pour augmenter la persistance intra-articulaire et l’antalgie de l’acide hyaluronique.
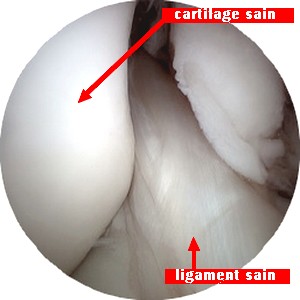 Ainsi sont résumées très vite plus de 120 ans de recherche sur une substance naturelle dont on connait la lente dégradation dans l’arthrose mais aussi dans tous les tissus de l’organisme du fait du vieillissement, des agressions oxydatives de l’environnement comme par exemple les ultra-violets sur la peau. Il se dit qu’à 50 ans l’homme a perdu 50% de son capital acide hyaluronique qui n’est que 20 grammes environ.
Ainsi sont résumées très vite plus de 120 ans de recherche sur une substance naturelle dont on connait la lente dégradation dans l’arthrose mais aussi dans tous les tissus de l’organisme du fait du vieillissement, des agressions oxydatives de l’environnement comme par exemple les ultra-violets sur la peau. Il se dit qu’à 50 ans l’homme a perdu 50% de son capital acide hyaluronique qui n’est que 20 grammes environ.
Ce survol pour atterrir sur la viscosupplémentation a volontairement ignoré beaucoup d’autres actions de l’acide hyaluronique dans l’organisme et concernant notamment la cicatrisation, l’hydratation ou la migration cellulaire pour ne retenir que ce qui a permis à ce concept de voir le jour.