Mannitol, réticulation, les garde-chaines des hyaluronates dans l’arthrose.
Dans de nombreuses indications médicales le mannitol est associé au hyaluronate de sodium parce qu’il a un grand pouvoir anti radicalaire du fait de la présence de 10 radicaux hydroxyle dans sa molécule. C’est le cas de certaines préparations viscoélastiques à visée ophtalmologique où l’endothélium cornéen est ainsi protégé du stress oxydatif directement lié à l’injection et le viscosupplément est plus résistant à l’attaque des radicaux libres présents dans le milieu (1). De la même manière dans d’autres utilisations médicales. Dans d’autres indications oculaires c’est la réticulation du hyaluronate qui apporte une solution à certaines pathologies comme pour l’enophtalmie qui nécessite un gel extrêmement réticulé. Aujourd’hui, dans les mêmes conditions de réflexion, la préparation de viscosuppléments à visée articulaire doit répondre aux quelques faiblesses connues des produits efficaces anciens. En introduisant un anti oxydant et une certaine proportion de réticulation, en adaptant le volume et la concentration du gel à l’articulation à traiter, on « mesure » le viscosupplément nécessaire à obtention du résultat optimal.
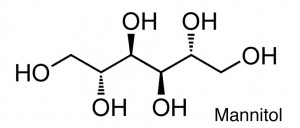
Le mannitol
C’est un sucre-alcool, polyol utilisé depuis très longtemps comme conservateur et qui a fait preuve de son excellente tolérance dans l’organisme humain à des doses très élevées. Il régule l’osmolarité des différents milieux liquides. Le mannitol est d’origine naturelle : on le trouve ainsi à concentrations élevées dans des végétaux comme le frêne, le framboisier, dans des légumes comme le céleri, la carotte, dans les algues marines et dans les champignons comme le Cordyceps sinensis (l’or brun du Tibet).
Il possède un grand pouvoir anti radicalaire (2). Il a la capacité de protéger les molécules notamment des radiations ionisantes et des agressions chimiques comme celle les radicaux libres. Il constitue une référence dans cette action. Cette capacité a été étudiée en association à l’acide hyaluronique au cours de l’inflammation synoviale (3) : la dégradation oxydative de la chaine est d’autant plus inhibée par le mannitol que sa concentration est plus élevée. Cette action anti-radicalaire lui confère une action anti-inflammatoire et analgésique propre qui s’ajoute à celle connue de l’acide hyaluronique (hyaluronate).
Très hydrosoluble, le mannitol a aussi le pouvoir de stabiliser les structures physicochimiques des protéines et des glycosaminoglycanes en renforçant par exemple les liaisons hydrophobes ce qui augmente leur résistance à de fortes températures (4) comme celles qu’impose la stérilisation par autoclavage des hyaluronates avant leur utilisation thérapeutique. Le polyol est lui-même parfaitement résistant à cette épreuve à la différence de nombreux autres anti oxydants comme la vitamine C ou les polyphénols qui sont détruits par la chaleur.
Enfin l’adjonction de mannitol dans une préparation de hyaluronate confère une grande stabilité aux propriétés rhéologiques développées pour un viscosupplément à température ambiante. Comme il participe à l’équilibre osmolaire des milieux dans lesquels il est inclus, il permet de diminuer la concentration en sel (Na Cl) nécessaire à l’iso tonicité des solutions injectables de hyaluronate de sodium et optimise de déploiement spatial des chaines sucrées dans le gel.
Le mannitol jouit d’une innocuité quasi-totale prouvée par de nombreux essais. Il n’est pas cytotoxique ou cancérigène. Il est dépourvu d’effet génétique et n’est pas mutagène. Il n’est pas toxique même à de très fortes doses. Il est utilisé par voie intraveineuse comme diurétique osmotique à raison de 100 g. en solution hyper osmolaire à 10-20% sur 4 à 8 heures dans les insuffisances rénales pour augmenter la diurèse. Par voie sous-cutanée c’est un outil utilisé dans la deshydratation du nourrisson. C’est aussi un des traitements des œdèmes cérébraux ou de l’hypertension intra oculaire.
Comme le sorbitol, son isomère, il est prescrit à raison de 20 g. par jour pour son pouvoir laxatif. Enfin c’est un édulcorant naturel utilisé par les diabétiques à la place du glucose.
La réticulation
L’acide hyaluronique (hyaluronate) est le « porteur d’eau » de notre organisme. Il a été isolé en 1934 par Karl Meyer et John Palmer. Il est aussi appelé hyaluronane par assimilation à la famille des glycosaminoglycanes dont il fait partie. Il maintient un bon niveau d’hydratation des tissus en la fixant entre ses chaines. Un gramme d’AH libre peut retenir jusqu’à 1 kilogramme donc 1 litre d’eau. La quantité et la qualité diminuent dans le cartilage au cours de l’arthrose. L’AH est aussi un capteur de radicaux libres par ses fonctions hydroxyles et à ce titre a une certaine action anti-inflammatoire et donc antalgique mais il n’est utilisé en médecine que pour ses propriétés viscoélastiques reconnues et non pour ses propriétés pharmacologiques probables.
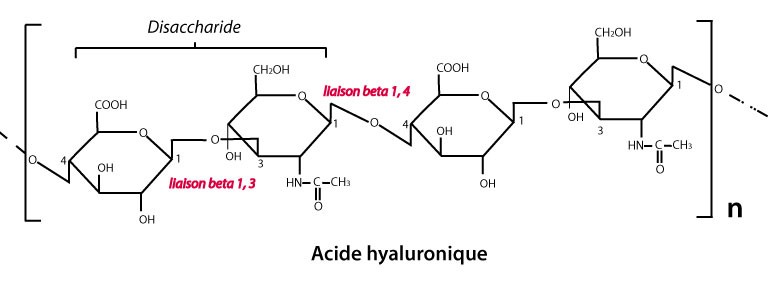
Il correspond à une chaine comportant dans chaque maillon deux disaccaharides (chacun formé d’un acide glucuronique relié à une N-acétyl-glucosamine par une liaison β 1-3) reliés entre eux par une liaison β 1-4. Cette alternance de liaison β 1-3 et β 1-4 est spécifique à la molécule. Le nombre de maillons n se situe autour de 2500 dans les conditions physiologiques normales et va déterminer son poids moléculaire (PM). L’acide hyaluronique « natif » a un PM de 2.5 à 10 millions de Daltons. Dans une articulation cette constante varie de 0.5 à 4 millions de Daltons selon l’état local. Sa destruction est régulièrement assurée par des hyaluronidases endogènes. La fabrication dont les propriétés rhéologiques et la destruction sont régulées au sein des différents tissus par des récepteurs cellulaires. C’est cette régulation variable entre différents individus qui pourrait expliquer certains échecs thérapeutiques avec une catégorie possible de « destructeurs rapides » (5)
Na-Glucuronate N-Acétyl-glucosamine
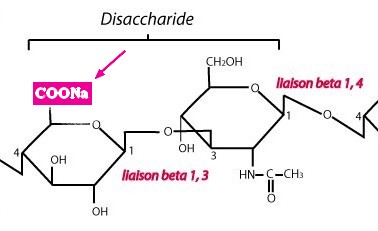
Physiologiquement il est sous la forme d’un sel sodique, le hyaluronate de sodium où le H de la fonction acide COOH en 6 de l’acide glucuronique est remplacé par un atome de sodium Na.
L’acide hyaluronique exogène utilisé comme viscosupplément peut être issu de deux sources différentes. Il est soit d’origine animale extrait alors de la crête de coq, soit d’origine non animale et obtenu par fermentation bactérienne à partir d’une souche de streptocoque non pathogène pour l’homme : streptococcus equi. Il est important de savoir que les molécules d’acide hyaluronique (hyaluronate) n’ont aucune spécificité de tissu mais aussi d’espèce dans le monde animal : il n’y a donc pas de risque théorique d’allergies. Cependant comme le produit est par exemple obtenu à partir de tissus aviaires comme la crête de coq, il est toujours possible, et ce malgré les traitements chimiques et les filtrations multiples auxquels sont soumis ces extraits, de voir un fragment protéique, alors étranger à l’homme, rester fixé à la chaine d’acide hyaluronique (hyaluronate) alors très rarement responsable alors d’une réaction immuno-allergique chez un sujet sensible.
L’acide hyaluronique (hyaluronate), on l’a déjà précisé, a la capacité de retenir fortement l’eau. Cette qualité contribue au maintien de la cohésion et de la structure du cartilage articulaire et participe à obtention des propriétés viscoélastiques de ce tissu « mécanique ». Dans sa forme naturelle, l’acide hyaluronique (hyaluronate) est à l’état libre non réticulé. C’est une transformation physico-chimique qui va permettre d’obtenir un gel viscoélastique plus ou moins dense selon le nombre imposé de liaisons entre les chaines et intéressant les radicaux carboxyle et hydroxyle. Un agent chimique, le BDDE, va créer ces « ponts » et une structure tridimensionnelle à partir des chaines libres d’acide hyaluronique (hyaluronate) préalablement préparées par linéarisation.
Cette réticulation va intéresser une proportion variable de chaines selon le produit final que l’on veut obtenir. Une transformation légère de 1% des chaines correspond à une stabilisation. Le produit ainsi obtenu pourra être mélangé avec à une préparation plus fortement réticulée créant des conditions optimales pour certaines indications de viscosupplémentation.
Les différences entre les produits obtenus par cette méthode vont dépendre notamment du PM des AH choisis, de la concentration d’AH qui ne peut dépasser 25 mg par ml, du nombre de ponts et de l’intensité des liaisons générés par la réticulation. On obtient ainsi des produits finis qui se différencieront par leur viscosité ou résistance à l’écoulement uniforme et sans turbulence (la capacité à l’écoulement d’un fluide diminue quand la viscosité augmente), leur élasticité (la capacité d’un objet à être déformable tout en reprenant sa forme d’origine lorsque la contrainte qu’on lui applique disparait) et leur cohésivité (capacité d’une matière à conserver sa stabilité par le jeu des forces intérieures.). Globalement plus le produit est réticulé, plus il est visqueux passant à l’état de gel puis de solide et utilisé dans cette forme comme membrane biologique, cela se faisant au détriment de l’élasticité. Plus les liaisons entre chaines seront nombreuses plus le viscosupplément va durer et résister à la dégradation oxydative et enzymatique naturelle. Le schéma ci-dessous rend compte des différentes formes que peuvent prendre les chaines acide hyaluronique (hyaluronate) : linéaire libre et réticulé
Au total
L’adjonction de mannitol au pouvoir antioxydant à un viscosupplément renforce ses capacités à lutter contre la dégradation oxydative, augmente le pouvoir antalgique de la préparation. Un certain degré de réticulation apporte une meilleure résistance des chaines d’AH à sa dégradation par les hyaluronidases et les radicaux libres présents dans le milieu où il est injecté tout en conservant au viscosupplément les propriétés rhéologiques les plus physiologiques possibles.
Entre le viscosupplément d’AH linéaire simple de bas poids moléculaire et la véritable « soupe de pates « lettres » » obtenue par procédé Nasha incluant des microsphères d’AH réticulé dans une solution d’AH non réticulé qui correspondent aux extrêmes des AH d’hier, on a aujourd’hui à notre disposition des préparations viscoélastiques de nouvelle génération mieux pensées et plus élaborées. On peut désormais envisager une meilleure prise en charge des diverses articulations atteintes d’arthrose.
Bibliographie
1-Belda U. et al. HA combined with mannitol to improve protection against free-radical endothelial damage : experimental method. J. Cataract.Ref.Surg. 31,2005, 1213-18
2-Elena Fratia, Abdel-Majid Khatiba,Philippe Fronta,Andrej Panasyuka,France Aprilea,Dragoslav R. Mitrovic. Degradation of Hyaluronic Acid by Photosensitized Riboflavin In Vitro. Modulation of the Effect by Transition Metals, Radical Quenchers, and Metal Chelators. Free Radical Biology and Medicine, 22, 1997, 1139–44
3-Gracia Mendoza,Ana I. Álvarez,Mivis M. Pulido,Antonio J. Molina,Gracia Merino,Rebeca Real,Peter Fernandes,Julio G. Prieto. Inhibitory effects of different antioxidants on hyaluronan depolymerization. Carbohydrate Research,342 ( 1), 2007, 96–102.
4- Joan F. Back , David Oakenfull , Malcolm B. Smith. Increased thermal stability of proteins in the presence of sugars and polyols. Biochemistry, 1979, 18 (23), 5191–96.
5. P. Micheels, SJ Saint Hillier. Hyaluronane et derme: réflexions et mises au point. J.Med. et Chir.Derm. XXXV, 158, 2008,81-85.








2 commentaires
Marie a écrit:
24 mar 2015
Bonjour,
« Mannitol, réticulation, les garde-chaines des hyaluronates dans l’arthrose ».(2ième génération)
Ce produit est-il à l’essai ou bien peut-on se le procurer chez le pharmacien ?. Dans ce cas, comment se nomme le produit ?
Merci d’avance
cordialement
medecin42140 a écrit:
24 mar 2015
Vous trouverez ces viscosuppléments de 2* génération en vous adressant directement notamment au laboratoire Labrha qui les commercialise ou en les demandant à votre rhumatologue ou autre médecin spécialiste qualifié pour les utiliser, lequel vous donnera un bon de commande. Les différents produits proposés sont adaptés aux différentes articulations (Happycross, Happymini: voir dans le site les articles les concernant)