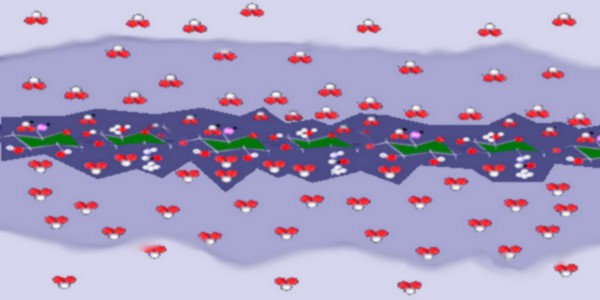
L’hydratation de l’acide hyaluronique est la clé de ses propriétés visco-élastiques.
Un rappel de sa structure, de sa fabrication et de son rôle.
L’acide hyaluronique ou AH est un glycosaminoglycane très particulier car il existe à l’état libre, sans liaison aux protéines à la différence des protéoglycanes, autres constituants de la matière extracellulaire (MEC). En plus il n’est jamais sulfaté comme peuvent l’être d’autres glycosaminoglycanes (chondroïtine sulfate ou héparine sulfate ou encore kératane sulfate). Il forme une chaîne polysaccharidique de très grande taille par polymérisation de centaines d’unités disaccharidiques liées en β (1 4) par des HA synthases au nombre de 3 (HAS1, HAS2 et HAS3) donnant des familles de AH à longueur de chaîne et propriétés physiologiques différentes. Chaque unité sucrée est un motif β-GlcA (acide glucuronique)-(1 3)-GlcNAc(N acetyl glucosamine).
Sa synthèse remarquable, car unique, se fait au niveau de la membrane plasmique par intervention des HAS et extrudation d’un polymère en voie de formation vers la MEC. Le HA va ensuite servir de support pour la fixation de chaînes de protéoglycanes sulfatés créant un réseau supramoléculaire de taille considérable capable de fixer de grandes quantités de molécules d’eau et ions divers qui maintiennent l’hydratation et la tonicité tissulaire.
L’AH est reconnu des cellules par certains de ses récepteurs membranaires en particulier le CD44 qui activent une succession de signaux intracellulaires régulateurs de leur prolifération, migration et différenciation. La réponse cellulaire est dépendante de la taille du HA qui est évaluée par les récepteurs mais aussi de celle des polymères de dégradation provenant de l’action enzymatique des hyaluronidases et de celle, oxydative, des radicaux libres. L’acide hyaluronique est métaboliquement extrêmement actif, se renouvelle en permanence et a une durée de vie très courte de l’ordre du jour au niveau de la peau par exemple.
L’AH forme de très longues chaines flexibles et hélicoïdales avec des spires comprenant quatre unités disaccharidiques et pouvant atteindre des dizaines de micromètres de longueur. Selon le type des liquides biologiques, les chaines adoptent des figures différentes, s’étalant ou se repliant par exemple en fonction de la salinité du milieu. La tendance pour la molécule reste toutefois à l’occupation du plus grand volume spatial. Ainsi à l’état hydraté, 1 g d’AH peut « occuper » un volume de 1000 cm3 ce qui ne signifie pas qu’il fixe 1 litre d’eau comme on le verra ensuite.
Selon les contraintes de pression imposées à l’AH, les chaines peuvent se lier entre elles, se dérouler ou se pelotonner adoptant ainsi des capacités visco-élastiques variables. C’est une des propriétés essentielles de ce polymère pour les articulations qui sont ainsi protégées notamment des chocs.
On trouve l’AH dans tout le monde animal sans spécificité d’espèce. Il est aussi présent dans la capsule de certaines bactéries comme le streptocoque qui le synthétise. La gelée interne de la crête de coq en contient jusqu’à 7,5 mg/ml. Chez l’homme, il est particulièrement abondant,anecdotiquement, dans le cordon ombilical comme composant de la gelée de Wharton mais au premier chef dans la peau. On connait aussi sa présence en très grandes quantités dans l’humeur vitrée de l’œil d’où il tire son nom et dans le liquide synovial des articulations dont il est l’agent lubrifiant avec une concentration élevée de 2,5 à 4 g/l. C’est ce qui intéresse notre site. Il est moins abondant mais présent dans le cartilage et dans l’ensemble des tissus conjonctifs. Le poids moléculaire (PM) de la chaine d’AH peut varier selon les espèces : ainsi le rat-taupe fabrique un AH de très haut PM: 5 fois plus élevé que celui trouvé en moyenne chez l’homme.
L’hydratation de l’acide hyaluronique est la clé de ses propriétés visco-élastiques.
La chaîne d’AH, on l’a vu, est un long ruban tapissé de groupements –OH, de radicaux amines [-NH-CO-] et d’atomes d’oxygène formant les liaisons entre les sucres et entrant dans la composition des hexoses. Les atomes d’hydrogène, d’oxygène et d’azote ainsi présents vont retenir les molécules d’eau qui sont proches dans le milieu ambiant par des liaisons hydrogène. Mais aussi les radicaux carboxyle [-COO-] par leurs atomes d’oxygène participent à cette hydratation de la chaîne. 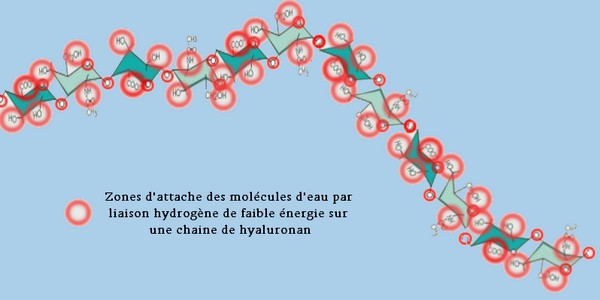 Les liaisons hydrogène sont favorisées par le caractère dipolaire non linéaire de la molécule d’eau qui a un angle de 104° entre les deux hydrogènes quand l’oxygène en est le sommet. Ainsi une simple molécule d’eau peut contracter des liaisons hydrogène avec 4 molécules d’eau voisines.
Les liaisons hydrogène sont favorisées par le caractère dipolaire non linéaire de la molécule d’eau qui a un angle de 104° entre les deux hydrogènes quand l’oxygène en est le sommet. Ainsi une simple molécule d’eau peut contracter des liaisons hydrogène avec 4 molécules d’eau voisines. 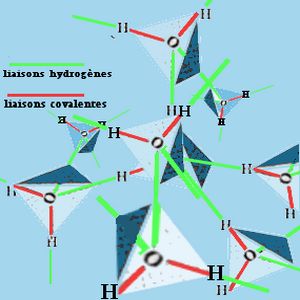 En plus les groupements à charge négative attirent des ions positifs comme Na+ qui sont eux même entourés de molécules d’eau. Ainsi se forme un manchon d’eau liée à la molécule non congelable.
En plus les groupements à charge négative attirent des ions positifs comme Na+ qui sont eux même entourés de molécules d’eau. Ainsi se forme un manchon d’eau liée à la molécule non congelable. 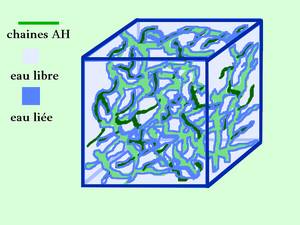 Puis l’eau va s’agglutiner autour de la chaîne par des liaisons hydrogène qui se forment de proche en proche entre les molécules créant un nuage d’hydratation en réseau continu comme celui que l’on trouve autour des chaines protéiques: c’est l’eau structurée qui voisine avec l’eau libre. Le poids d’eau liée retenu par la molécule est grossièrement de 1 gramme pour 1 gramme de chaîne d’AH. Ceci est donc totalement différent de la place que l’AH peut prendre dans un volume aqueux lorsque les conditions optimales sont requises pour qu’il étale dans les trois dimensions d’un espace donné. On a vu ainsi plus haut qu’un gramme d’AH pouvait alors occuper l’espace pris par un litre d’eau. Les chaines d’AH ne peuvent pas se replier et se recroqueviller, elles ont tendance à s’étendre dans l’espace. Elles vont ainsi former un gel hydrophile occupant un espace bien plus imposant que celui qu’occuperaient les polysaccharides seuls.
Puis l’eau va s’agglutiner autour de la chaîne par des liaisons hydrogène qui se forment de proche en proche entre les molécules créant un nuage d’hydratation en réseau continu comme celui que l’on trouve autour des chaines protéiques: c’est l’eau structurée qui voisine avec l’eau libre. Le poids d’eau liée retenu par la molécule est grossièrement de 1 gramme pour 1 gramme de chaîne d’AH. Ceci est donc totalement différent de la place que l’AH peut prendre dans un volume aqueux lorsque les conditions optimales sont requises pour qu’il étale dans les trois dimensions d’un espace donné. On a vu ainsi plus haut qu’un gramme d’AH pouvait alors occuper l’espace pris par un litre d’eau. Les chaines d’AH ne peuvent pas se replier et se recroqueviller, elles ont tendance à s’étendre dans l’espace. Elles vont ainsi former un gel hydrophile occupant un espace bien plus imposant que celui qu’occuperaient les polysaccharides seuls.
C’est cette forte hydratation de l’AH qui explique les propriétés mécaniques visco-élastiques et lubrifiantes de l’AH. Une pression importante de l’extérieur peut casser des liaisons hydrogène qui, si elles sont donc fragiles, se reforment aussi dès la disparition de la contrainte. Ainsi les phases de déshydratation succède à celles d’hydratation comme les actions d’amortissement suivi de celles de résistance.